类 器官技术“爆红”的背后,是“赶时髦”科研还是有“真材实料”呢?
类器官不是器官
一直以来,“类器官”一词被宽泛地用于所有来源于原代组织 (组织亚基或单细胞)、胚胎干细胞 (ESCs) 和诱导多能干细胞 (iPSCs)、已建立的细胞系以及完整或分段器官 (如由多种组织类型组成的器官外植体) 的三维 (3D) 器官型培养。
我们可以这样理解,类器官是完全由原代组织、ESCs 或 iPSCs 衍生而来的体外 3D 细胞簇,它们具有自我更新和自组织能力,并表现出与起源组织相似的器官功能。
“爆红”绝非偶然
其实,3D 类器官培养是在上个世纪建立和发展起来的。早在 1907 年,Wilson 等人首次表明,分离的海绵细胞能够自组织再生成整个生物体。2009 年,Hans Clevers 和同事在肠道类器官培养系统中取得突破性进展,开启了类器官技术的发展“新纪元”。
目前,已有方法可以构建肝脏、结肠、肠道、肾脏、肺、前列腺、胰腺、胃、大脑皮层和视网膜等多种组织的类器官。体外类器官 模型 是一项重大的技术突破,它为研究组织发育、疾病建模、药物筛选、个性化医学和细胞治疗提供了一个强大的工具 。
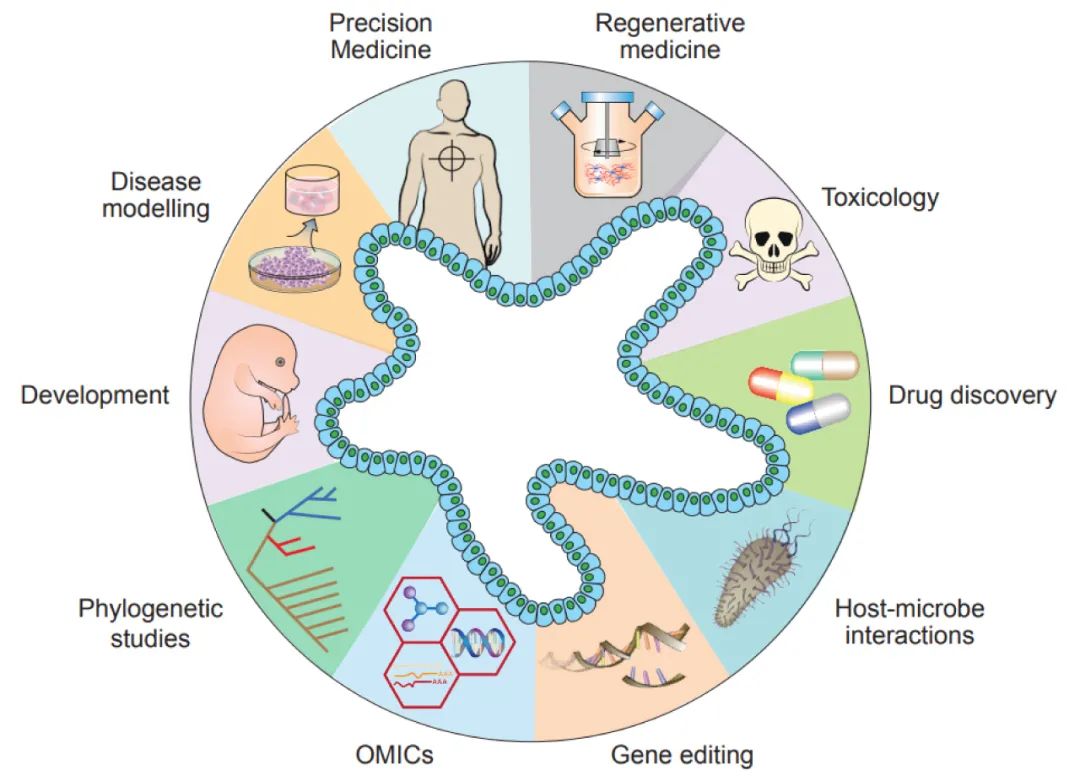
图 1. 类器官技术的多样化应用[2]
■ 与传统细胞培养及动物模型对比,其秀在何处?
1) 与传统的体外培养不同,类器官在组成和结构上与原代组织 (Primary tissue) 相似:包含了少量基因组稳定、自我更新的干细胞,这些子代的细胞谱系与活组织的主要细胞谱系相似;
2) 类器官可以快速扩增、冷冻保存,且能应用于高通量分析;
3) 原发组织来源的类器官缺乏间充质/间质,为研究感兴趣的组织类型提供了一种简化的途径,而不受局部微环境的干扰;
4) 类器官是传统 2D 培养和体内小鼠模型之间的重要桥梁,因为它们比单层培养模型更具有生理相关性,而且比体内模型更易于操纵生态位成分、信号通路和基因组编辑。
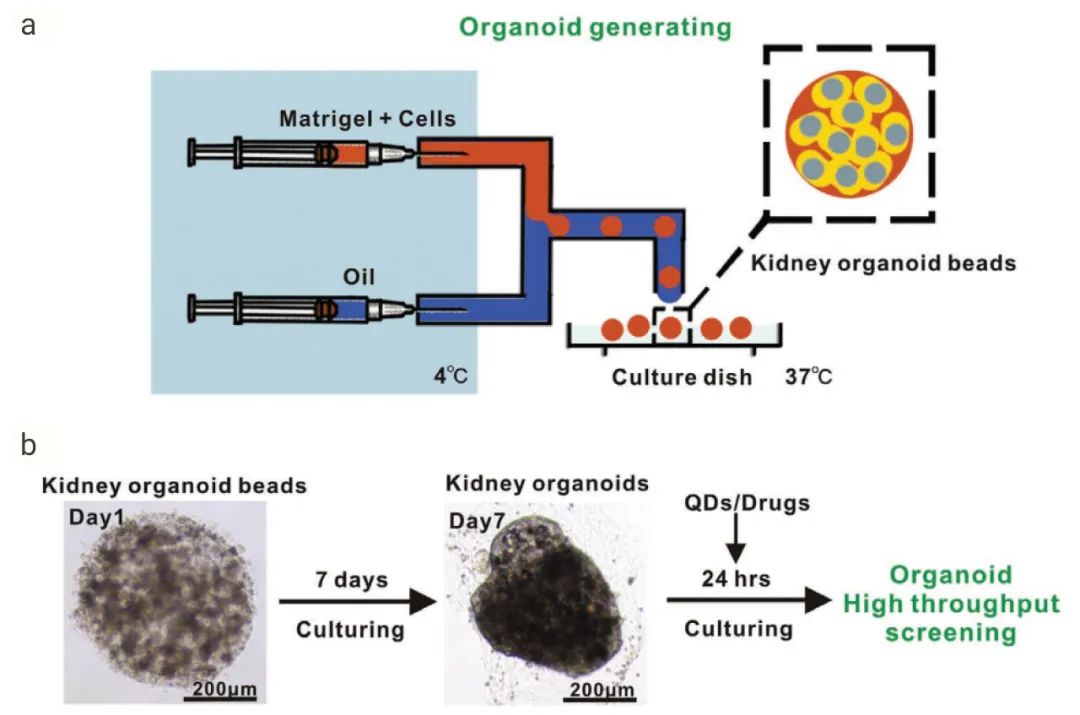
图 2. 建立小鼠可再生的肾类器官应用于肾毒性剂量定量筛选[12]
文中所用 Noggin, R-spondin 1, SB431542, CHIR99021,
武汉格发信息技术有限公司,格发许可优化管理系统可以帮你评估贵公司软件许可的真实需求,再低成本合规性管理软件许可,帮助贵司提高软件投资回报率,为软件采购、使用提供科学决策依据。支持的软件有: CAD,CAE,PDM,PLM,Catia,Ugnx, AutoCAD, Pro/E, Solidworks 等。